اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از دستگاه QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase
اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از دستگاه QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase

مطالعه بالینی: اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از طیفسنجی پرقدرت زمان-پرواز برای غلبه بر تداخلها پس از تجویز گلوکارپیداز
بخش اول: مقدمه
متوترکسات (MTX) یک آنتاگونیست اسید فولیک با خاصیت ضدتکثیری است.
افزون بر فعالیت ضدسرطانی، این دارو دارای اثرات تنظیمکننده سیستم ایمنی و ضدالتهابی نیز هست؛ بنابراین در درمان بیماریهای هماتولوژیک و دیگر بیماریها، در دوزهای مختلف کاربرد دارد.
درمان با دوز بالای متوترکسات نیازمند پایش دقیق سطح دارو در خون است تا از حذف مناسب آن اطمینان حاصل شود.
یکی از عوارض احتمالی این درمان، نارسایی کلیوی است که باعث تجمع دارو و افزایش سمیت میشود.
علیرغم تمام اقدامات پیشگیرانه، تا ۱.۸٪ از بیماران دچار آسیب کلیوی ناشی از رسوب بلورهای MTX و متابولیت آن، ۷-هیدروکسیمتوترکسات (7-OH-MTX)، در لولههای کلیوی میشوند. در این گروه، میزان مرگومیر حدود ۴٪ گزارش شده است.
دفع تأخیری متوترکسات میتواند به عوارضی همچون سرکوب مغز استخوان یا التهاب مخاط دهان منجر شود. به همین دلیل، سطح دارو باید هر ۲۴ ساعت پایش شود تا زمانی که به زیر ۰.۱ میکرومول در لیتر برسد.
در زمینه اندازهگیری داروی متوترکسات (Methotrexate) و متابولیتهای آن در سرم بیماران، بهویژه در شرایط نارسایی کلیوی و پس از درمان با گلوکارپیداز (Glucarpidase) است. این مقاله از لحاظ بالینی، تحلیلی و فنی بسیار دقیق بوده و به بررسی روش LC-UHR-QTOF جهت سنجش دقیق این ترکیبات میپردازد.
بخش دوم: درمان با گلوکارپیداز و مشکل تداخل DAMPA
در کنار تجویز لوسوورین (اسید فولینیک) بهعنوان درمان مکمل، روشهایی مانند دیالیز با فیلتراسیون بالا، همودیافیلتراسیون مداوم، تیمیدین و گلوکارپیداز برای کاهش سطح MTX به کار میروند.
گلوکارپیداز (شکل نوترکیب آنزیم Carboxypeptidase-G2)، دارویی است که به سرعت سطح متوترکسات را در سرم کاهش میدهد (۹۵–۹۹٪ طی ۱۵ تا ۳۰ دقیقه). این دارو با نام تجاری Voraxaze® شناخته میشود و از سال ۲۰۱۲ توسط FDA برای درمان سطوح سمی MTX (بیش از ۱ µM) در بیماران با اختلال عملکرد کلیه تأیید شده است. این آنزیم متوترکسات را به گلوتامات و متابولیت غیرفعال DAMPA (2,4-diamino-N10-methylpteroic acid) تجزیه میکند.
یکی از چالشهای عمده این درمان، تداخل متابولیت DAMPA با روشهای ایمنیسنجی (immunoassay) رایج در آزمایشگاههاست، که منجر به تخمین بیش از حد غلظت MTX میشود. این تداخل حدود ۴۸ ساعت باقی میماند و باعث میشود روشهای ایمونواسی برای سنجش دقیق در این مدت قابل اعتماد نباشند.
🧪 بخش سوم: گزارش مورد بالینی
شرح مورد بالینی
زنی ۴۷ ساله با تشخیص لوسمی لنفوبلاستیک حاد نوع B (ALL-B)، طبق پروتکل درمانی PETHEMA ALL-AR-03 در بیمارستان بستری شد. در ابتدا این بیمار به عنوان مورد مشکوک به نارسایی کلیه مورد بررسی قرار گرفت.
تزریق دوز بالای اولیه متوترکسات (۳ گرم به ازای هر مترمربع سطح بدن، بهصورت انفوزیون وریدی طی ۲۴ ساعت) بهخوبی تحمل شده بود.
اما پس از دوره دوم درمان، سطح کراتینین سرم از ۳۷.۱۳ به ۲۹۱.۷۳ میکرومول در لیتر افزایش یافت.
نرخ فیلتراسیون گلومرولی تخمینزدهشده (GFR) معادل ۱۵.۰۵ میلیلیتر بر دقیقه (بر اساس روش گروه مطالعه رژیم غذایی در بیماری کلیه – ایزوتوپ رقیقسازی جرمی) بود که نشاندهنده نارسایی کلیه است.
دفع متوترکسات کاهش یافته بود و این موضوع منجر به تجمع سمی آن با غلظت ۵۷.۴۷ میلیگرم بر دسیلیتر پس از ۳۶ ساعت از تزریق دارو شد.
براساس دستورالعمل، در شرایط نارسایی کلیه اگر غلظت MTX بیش از ۱۰ میکرومول در لیتر و/یا کراتینین بالاتر از ۱۳۲.۶ میکرومول باشد، درمان با گلوکارپیداز توصیه میشود. این بیمار هر دو شرط را داشت.
طرح درمانی شامل تجویز ۵۰ واحد به ازای هر کیلوگرم از دارو به صورت تزریق وریدی طی ۵ دقیقه بود. پیش از آن، تجویز اسید فولینیک متوقف شد زیرا سوبسترای آنزیم است. سطوح متوترکسات به ترتیب در زمانهای ۱۵، ۳۰ و ۶۰ دقیقه پس از تزریق گلوکارپیداز، با روش ایمونواسی مرجع آزمایشگاهی اندازهگیری شد.
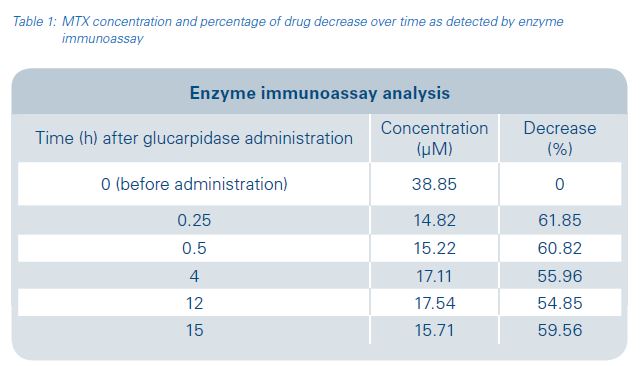
نتایج: کاهش ۶۱.۸۵٪ در سطح متوترکسات در ۱۵ دقیقه اول مشاهده شد (جدول ۱). این کاهش کمتر از میزان مورد انتظار بود و علت آن تداخل متابولیت DAMPA در روش ایمونواسی ذکر شده است.
📉 جدول ۱ – غلظت متوترکسات در روش ایمونواسی
| زمان (ساعت) | غلظت (μM) | درصد کاهش (%) |
| ۰ (قبل درمان) | ۳۸.۸۵ | ۰ |
| ۰.۲۵ | ۱۴.۸۲ | ۶۱.۸۵ |
| ۰.۵ | ۱۵.۲۲ | ۶۰.۸۲ |
| ۴ | ۱۷.۱۱ | ۵۵.۹۶ |
| ۱۲ | ۱۷.۵۴ | ۵۴.۸۵ |
| ۱۵ | ۱۵.۷۱ | ۵۹.۵۶ |
💉 درمانهای بعدی
پس از ۴۸ ساعت، تصمیم بالینی بر آن شد که بیمار تحت درمان پاکسازی برونتنی (extracorporeal) قرار گیرد تا بقایای MTX و بهبود عملکرد کلیوی حاصل شود.
روش انتخابی همودیافیلتراسیون آنلاین بود، چرا که در مطالعات قبلی بهعنوان مؤثرترین روش معرفی شده بود.
دوز دوم گلوکارپیداز تجویز نشد زیرا اثربخشی آن در این زمینه نامشخص بود.
درمان همودیافیلتراسیون تا زمانی ادامه یافت که سطح MTX (بر اساس روش ایمونواسی) به زیر ۰.۱۰ میکرومول در لیتر رسید.
🧬 بخش چهارم: پارامترهای کروماتوگرافی و طیفسنجی
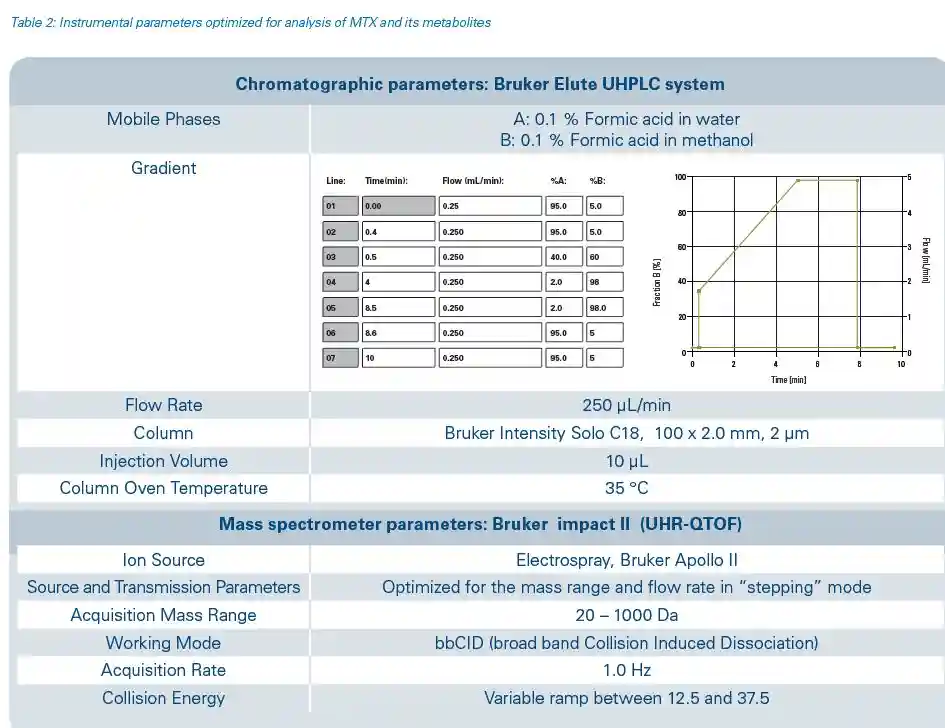
💧 دستگاه کروماتوگرافی UHPLC Bruker Elute
- فازهای متحرک:
- A: اسید فرمیک ۰.۱٪ در آب
- B: اسید فرمیک ۰.۱٪ در متانول
- گرادیان جریان:
- زمان کل: ۱۰ دقیقه
- نرخ جریان: ۰.۲۵ میلیلیتر در دقیقه
- ستون: Bruker Intensity Solo C18، اندازه ۲×۱۰۰ میلیمتر، ذرات ۲ میکرونی
- دمای ستون: ۳۵ درجه سانتیگراد
- حجم تزریق: ۱۰ میکرولیتر
⚛️ طیفسنج جرمی UHR-QTOF (Bruker impact II)
- منبع یونسازی: الکترواسپری (Electrospray, Apollo II)
- محدوده جرمی: ۲۰ تا ۱۰۰۰ دالتون
- نرخ نمونهبرداری: ۱.۰ هرتز
- مد تحلیل: bbCID (برخورد القایی باند پهن)
- انرژی برخورد: رمپ متغیر از ۱۲.۵ تا ۳۷.۵ ولت
میدهم.
🧫 بخش پنجم: مواد و روشها
در طی درمان بیمار، اندازهگیری غلظت متوترکسات با استفاده از روش مرجع ایمونواسی آنزیمی (enzyme immunoassay) انجام شد که دارای حد تشخیص (LOD) برابر با ۰.۱۰ میکرومول در لیتر بود.
کیت مورد استفاده برای اندازهگیری غلظتهای بین ۰ تا ۲ میکرومول طراحی شده است. کنترلهای کیفی داخلی این روش، ضریب تغییرات (C.V.) برابر با ۹.۹۴٪ نشان دادند.
جمعآوری نمونهها:
نمونههای خون در لولههای مخصوص دارای فعالکننده لخته و جداکننده سرم جمعآوری شده و به مدت ۱۰ دقیقه با سرعت ۳۵۰۰ دور در دقیقه در دمای محیط سانتریفیوژ شدند.
💉 روش جایگزین تحلیلی: LC-UHR-QTOF
برای بررسی دقیقتر غلظت MTX، از روش کروماتوگرافی مایع با طیفسنجی جرمی پرتوان و فوقرزولوشن نوع QTOF استفاده شد. (Bruker Daltonics)
مراحل آمادهسازی نمونه:
- نمونههای سرم در دمای محیط ذوب شدند.
- با نسبت ۱ به ۱۰، متانول (درجه خلوص ۹۹.۸٪، شرکت Merck) برای رسوبزدایی پروتئینها به نمونه افزوده شد.
- مخلوطها ویortex شده و سپس به مدت ۲ دقیقه با سرعت ۱۳۰۰۰ دور در دقیقه سانتریفیوژ شدند.
- سوپرناتانت (مایع رویی) بدون هیچ تصفیه اضافی، با حجم ۱۰ میکرولیتر، تزریق مستقیم در سیستم LC-MS شد.
استانداردهای کالیبراسیون و کنترل کیفی کیت، همانند نمونهها آماده و اندازهگیری شدند.
📊 بخش ششم: نتایج و بحث
✅ مقایسه روش ایمونواسی و LC-UHR-QTOF
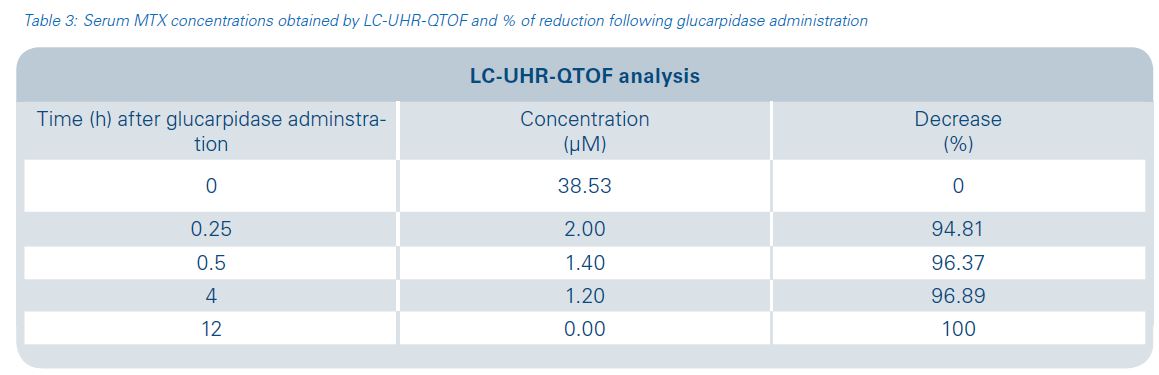
نتایج حاصل از LC-UHR-QTOF:
| زمان (ساعت) پس از تزریق گلوکارپیداز | غلظت MTX (μM) | درصد کاهش (%) |
| ۰ | ۳۸.۵۳ | ۰ |
| ۰.۲۵ | ۲.۰۰ | ۹۴.۸۱ |
| ۰.۵ | ۱.۴۰ | ۹۶.۳۷ |
| ۴ | ۱.۲۰ | ۹۶.۸۹ |
| ۱۲ | ۰.۰۰ | ۱۰۰ |
✳️ همانطور که جدول نشان میدهد، روش LC-UHR-QTOF توانست کاهش واقعی غلظت MTX را در مقایسه با روش ایمونواسی (که دچار تداخل متابولیت DAMPA است) با دقت بسیار بالا نشان دهد.
💡 ویژگیهای روش LC-UHR-QTOF:
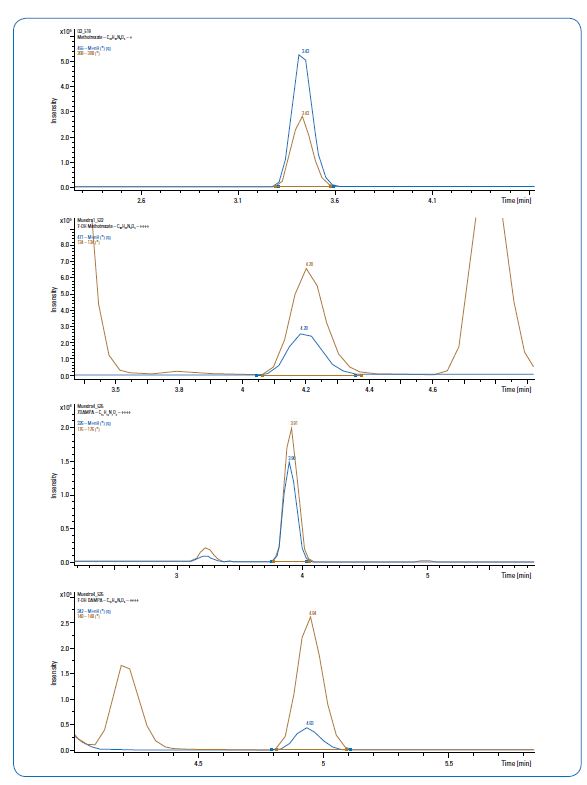
- قابلیت تشخیص و اندازهگیری انتخابی و دقیق متوترکسات، DAMPA و سایر متابولیتها از جمله 7-OH-MTX و 7-OH-DAMPA
- جمعآوری همزمان دادههای MS و MS/MS با استفاده از روش bbCID
- تعیین جرم دقیق یونهای پیشساز و محصولات با فیلتری به دقت ۳ mDa
- درستی زمان نگهداری در حد ± ۰.۱ دقیقه
- بررسی الگوی ایزوتوپی با انحراف استاندارد نسبی کمتر از ۵۰ mδ
یونهای اندازهگیریشده در مد مثبت:
- MTX: C₂₀H₂₃N₇O₅ → m/z = 455.1786
- DAMPA: C₁₅H₁₆N₇O₂ → m/z = 326.1360
- 7-OH-MTX: C₂₀H₂₃N₈O₆ → m/z = 471.1735
- 7-OH-DAMPA: C₁₅H₁₆N₇O₃ → m/z = 342.1309
📈 کالیبراسیون و صحت روش
- کالیبراسیون خارجی با غلظتهای ۰.۲، ۰.۵ و ۱ میکرومول در لیتر
- کنترلهای کیفی با غلظتهای ۰.۳۳۸، ۱.۵۳۰ و ۹.۳۷۰ میکرومول در لیتر
- R² = ۰.۹۹۸ برای منحنی کالیبراسیون
- نسبت سیگنال به نویز برای سطح ۰.۲ µM برابر با ۴۸۰ بود
- بنابراین:
- LOD = ۰.۰۰۱ μM
- LOQ = ۰.۰۰۴ μM
- بنابراین:
✳️ نیاز به استاندارد داخلی احساس نشد زیرا اثر ماتریس مشاهده نشد و برآورد با مدل Partial Least Square انجام شد.
📉 اختلاف بین دو روش اندازهگیری
روش ایمونواسی در ساعات اولیه پس از تزریق گلوکارپیداز، غلظت MTX را بسیار بیشتر از مقدار واقعی نشان داد. این امر ناشی از تداخل قابلتوجه DAMPA بود که در آن روش شناسایی نمیشود و بهاشتباه بهعنوان MTX گزارش میشود.
پس از گذشت ۴۸ ساعت، سطح DAMPA نیز کاهش یافت و تداخل پایان یافت.
🧾 بخش هفتم: نتیجهگیری
✅ درمان با گلوکارپیداز در این مورد انتخاب مناسبی بود و تنها با یک دوز، نتایج درمانی مؤثری حاصل شد.
❌ با این حال، روش ایمونواسی رایج در آزمایشگاهها به دلیل تداخل شدید متابولیت DAMPA، در این شرایط نامناسب و نادقیق بود.
✅ در مقابل، روش LC-UHR-QTOF به عنوان یک راهکار ایدهآل برای تعیین سریع و دقیق متوترکسات و متابولیتهای آن در سرم معرفی میشود. این روش نهتنها به حساسیت و انتخابپذیری بالا دست مییابد، بلکه نیاز به آمادهسازی پیچیده نمونه ندارد و هزینه تحلیل هر نمونه را بهشدت کاهش میدهد.
🔬 این فناوری، بهویژه دستگاه Bruker impact II، برای کاربردهای بالینی با نیاز به دقت بالا در محیطهای ماتریکسی پیچیده مثل سرم انسانی بسیار مناسب است.
روش اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از دستگاه QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase
متود اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از دستگاه QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase
روش تست اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از دستگاه QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase
سنجش و میزان اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از دستگاه QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase
طیف سنجی اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی آن در سرم انسانی با استفاده از دستگاه QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase
اندازهگیری متوترکسات methotrexate و متابولیتهای اصلی در سرم انسانی با استفاده از دستگاه Q-TOF برای مقابله بر تداخلها پس از تجویز گلوکارپیداز glucarpidase
آنالیز متوترکسات methotrexate و متابولیت اصلی آن در سرم انسانی با استفاده از دستگاه bruker QTOF برای غلبه بر تداخلها پس از تجویز گلوکارپیداز glucarpidase



دیدگاهتان را بنویسید